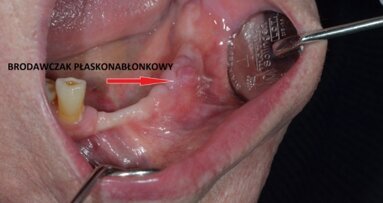
Wg doniesień z The Oral Cancer Foundation, wirusem brodawczaka ludzkiego (HPV), o którym wiadomo, że wywołuje kilka rodzajów nowotworów, zaraża się każdego dnia ok. 12 000 osób w wieku 15-24 lat. W nowym badaniu opartym na eksperymentach przedklinicznych, przeprowadzonym na Uniwersytecie Alabama w Birmingham (UAB) naukowcy sugerują, że leki przeciwnowotworowe vorinostat, belinostat i panobinostat mogą zostać ponownie wykorzystane w leczeniu zakażeń wywołanych przez HPV.
„Pilnie potrzebne są bezpieczne, skuteczne i niedrogie środki terapeutyczne” – powiedział prof. Sanjib Banerjee, adiunkt w dziedzinie biochemii i genetyki molekularnej w UAB i główny autor badania. Ponieważ nie można rozmnażać wirusa HPV w konwencjonalnej hodowli komórkowej, badanie jego patogennych skutków jest znacznie utrudnione. Prof. Louise Chow i prof. Thomas Broker z Wydziału Biochemii i Genetyki Molekularnej badali interakcje pomiędzy HPV a żywicielem od dziesięcioleci. Odkryli m.in., że program produkcyjny HPV zależy od zróżnicowania nabłonka. Dodatkowo, HPV reaktywuje replikację DNA gospodarza w tych zróżnicowanych komórkach w taki sposób, że białka replikacji i substraty stają się dostępne do wspierania amplifikacji wirusowego DNA.
W 2009 r. w tamtejszym laboratorium opracowano przełomowy model hodowli ludzkich keratynocytów zakażonych HPV-18, umożliwiając silną amplifikację DNA HPV-18 i wytwarzanie infekcyjnego wirusowego potomstwa. Zdaniem naukowców, ta produktywna hodowla ustanowiła idealny model do badań przedklinicznych potencjalnych leków przeciw HPV.
Mając to na uwadze, Banerjee i jego współpracownicy wysunęli hipotezę, że inhibitory deacetylaz histonowych (HDAC) będą hamować amplifikację DNA HPV z powodu ich znanego mechanizmu zakłócania replikacji chromosomalnego DNA. Replikacja chromosomowa wymaga zmian HDAC białek histonów – białek, które działają jak szpule niosące DNA, aby pomóc w pakowaniu i kondensacji chromosomów i genomu wirusowego. Vorinostat hamuje wiele HDAC, dlatego może nie tylko przerwać replikację chromosomów, ale także replikację wirusowego DNA.
Wykorzystując hodowle typu HPV-18, naukowcy odkryli, że vorinostat skutecznie hamuje amplifikację DNA HPV-18 i produkcję wirusów. Co istotne, vorinostat wywoływał zaprogramowaną śmierć komórki, zwaną apoptozą, we frakcji zróżnicowanych komórek. Śmierć można przypisać uszkodzeniu DNA po przerwaniu replikacji chromosomalnego DNA. Podobne wyniki uzyskano dla dodatkowych inhibitorów HDAC, belinostatu i panobinostatu. Zróżnicowane komórki niezakażonych hodowli, które nie replikują swojego DNA, zostały w znacznym stopniu oszczędzone w obecności inhibitorów. Zespół UAB zgłosił również, że vorinostat powodował rozległą śmierć komórek w hodowlach dysplastycznych i nowotworowych linii komórkowych niosących HPV-16.
„Na podstawie tych szczegółowych badań sugerujemy, że inhibitory HDAC są obiecującymi związkami do leczenia łagodnych zakażeń HPV, znosząc produkcję potomstwa i tym samym przerywając transmisję zakaźną” – powiedział Banerjee. Jedocześnie stwierdził, że niezbędne są dalsze badania w celu sprawdzenia, czy te środki mogą być również użyteczne w leczeniu dysplazji i nowotworów związanych z HPV.
Badanie „Vorinostat, inhibitor pan-HDAC, znosi produktywne wzmocnienie DNA HPV-18” zostało opublikowane w listopadzie 2018 r. w Proceedings of the National Academy of Sciences w USA.
HPV jest heterogenną grupą małych wirusów (52-55 nm) należących do rodziny papillomawirusów. Do tej pory zidentyfikowano ponad 170 ...
Tylko osoby cierpiące na migreny potrafią zrozumieć uciążliwość objawów tej choroby.
Tylko osoby cierpiące na migreny potrafią zrozumieć uciążliwość objawów tej choroby.
Co roku u ok. 650.000 osób zostaje zdiagnozowany nowotwór komórek nabłonka wielowarstwowego płaskiego głowy i szyi, a ok. 350.000 ...
Co roku u ok. 650.000 osób zostaje zdiagnozowany nowotwór komórek nabłonka wielowarstwowego płaskiego głowy i szyi, a ok. 350.000 ...
Wyniki najnowszych badań przeprowadzonych przez naukowców z University of Edinburgh, Peninsula Dental School, the University of Ottawa oraz UCL ...
Implanty zębowe stają się coraz bardziej powszechną metodą leczenia bezzębnych pacjentów, coraz ważniejsze staje się zrozumienie ich potencjalnych ...
Naukowcy z Gdańskiego Uniwersytetu Medycznego otrzymali patent na materiał, który pozwala na skuteczniejsze leczenie zakażeń kości. Hybrydowy ...
Kruszone lub sproszkowane skorupki jaj mają wiele praktycznych zastosowań. Można je stosować jako naturalny suplement wapnia, słodzik do kawy, lek na ...
Naukowcy opracowali eksperymentalną szczepionkę, która chroni do 80% myszy przed Staphylococcus aureus, bakterią Gram-dodatnią często występującą w...
Webinarium na żywo
czw. 2 kwietnia 2026
6:00 (CET) Warsaw
Webinarium na żywo
śro. 8 kwietnia 2026
7:00 (CET) Warsaw
Webinarium na żywo
czw. 9 kwietnia 2026
7:00 (CET) Warsaw
Webinarium na żywo
czw. 9 kwietnia 2026
8:00 (CET) Warsaw
Prof. Moritz Kebschull, Cat Edney
Webinarium na żywo
pią. 10 kwietnia 2026
4:00 (CET) Warsaw
Webinarium na żywo
pią. 10 kwietnia 2026
5:00 (CET) Warsaw
Dr. med. dent. Henrik-Christian Carl Hollay
Webinarium na żywo
pią. 10 kwietnia 2026
6:00 (CET) Warsaw
Prof. Dr. Ali Murat Kökat



 Austria / Österreich
Austria / Österreich
 Bośnia i Hercegowina / Босна и Херцеговина
Bośnia i Hercegowina / Босна и Херцеговина
 Bułgaria / България
Bułgaria / България
 Chorwacja / Hrvatska
Chorwacja / Hrvatska
 Czechy i Słowacja / Česká republika & Slovensko
Czechy i Słowacja / Česká republika & Slovensko
 Francja / France
Francja / France
 Niemcy / Deutschland
Niemcy / Deutschland
 Grecja / ΕΛΛΑΔΑ
Grecja / ΕΛΛΑΔΑ
 Węgry / Hungary
Węgry / Hungary
 Włochy / Italia
Włochy / Italia
 Holandia / Nederland
Holandia / Nederland
 nordycki / Nordic
nordycki / Nordic
 Polska / Polska
Polska / Polska
 Portugalia / Portugal
Portugalia / Portugal
 Rumunia i Mołdawia / România & Moldova
Rumunia i Mołdawia / România & Moldova
 Słowenia / Slovenija
Słowenia / Slovenija
 Serbia i Czarnogóra / Србија и Црна Гора
Serbia i Czarnogóra / Србија и Црна Гора
 Hiszpania / España
Hiszpania / España
 Szwajcaria / Schweiz
Szwajcaria / Schweiz
 indyk / Türkiye
indyk / Türkiye
 Wielka Brytania i Irlandia / UK & Ireland
Wielka Brytania i Irlandia / UK & Ireland
 Międzynarodowy / International
Międzynarodowy / International
 Brazylia / Brasil
Brazylia / Brasil
 Kanada / Canada
Kanada / Canada
 Ameryka Łacińska / Latinoamérica
Ameryka Łacińska / Latinoamérica
 USA / USA
USA / USA
 Chiny / 中国
Chiny / 中国
 Indie / भारत गणराज्य
Indie / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Wietnam / Việt Nam
Wietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Izrael / מְדִינַת יִשְׂרָאֵל
Izrael / מְדִינַת יִשְׂרָאֵל
 Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
 Bliski Wschód / Middle East
Bliski Wschód / Middle East