Agresywne formy zapalenia przyzębia związane z Aggregatibacter actinomycetemcomitans są często trudne do leczenia metodami tradycyjnymi, a w ostatnich latach opracowano bardzo niewiele nowych form terapii.
Ponieważ bakterie Aggregatibacter actinomycetemcomitans wytwarzają leukotoksynę, która zabija komórki odpornościowe gospodarza podczas infekcji, zmniejszając w ten sposób zdolność organizmu do zwalczania infekcji, naukowcy starają się opracować oparty na liposomach, reagujący na leukotoksynę nośnik antybiotyków do leczenia agresywnego zapalenia przyzębia u nastolatków. Wyniki pomogą stworzyć podstawy dla przyszłego rozwoju terapii skoncentrowanych na leukotoksynach.
Wg niedawnego raportu 4,95 mln zgonów rocznie jest związanych z opornymi bakteriami, a co najmniej 1,27 mln zgonów rocznie można bezpośrednio przypisać oporności na środki przeciwdrobnoustrojowe. Statystyki Centrum Kontroli i Prewencji Chorób (Centers for Disease Control and Prevention) pokazują, że tylko w USA każdego roku dochodzi do ponad 2,8 mln zakażeń opornych na środki przeciwdrobnoustrojowe, co prowadzi aż do ponad 35 000 zgonów.
Naukowcy z Lehigh University w USA otrzymali ostatnio grant od National Institutes of Health na opracowanie niechirurgicznego systemu dostarczania leków, który umożliwi kontrolowane podawanie antybiotyków w leczeniu agresywnego zapalenia przyzębia. W swoim projekcie wykorzystają model, który umożliwia wspólną hodowlę ludzkich komórek odpornościowych i komórek bakteryjnych. „Sposób, w jaki zwykle leczy się te infekcje polega na skalowaniu i struganiu, co zasadniczo oznacza zeskrobywanie bakterii, a następnie przepisywanie doustnych antybiotyków” – komentuje w komunikacie prasowym dr Angela Brown, adiunkt na Wydziale Inżynierii Chemicznej i Biomolekularnej na Lehigh University. „I chociaż zwykle to działa, czasami bakterie wracają, a potem trzeba zacząć od nowa antybiotykoterapię. Im częściej przyjmujesz antybiotyki, tym większe są szanse, że bakterie staną się na nie odporne”.
W swojej poprzedniej pracy naukowej dr Brown i jej zespół wykazali, że antybiotyki można zamknąć w liposomach i wykorzystać to jako mechanizm podawania leków. Ponadto wykazali, że leukotoksyna uwalniana przez bakterie wyzwala uwalnianie antybiotyków. „Leukotoksyna zwalcza odpowiedź immunologiczną organizmu, wiążąc się z cholesterolem w błonie białych krwinek, niszcząc błonę i zabijając komórki” – wyjaśnia dr Brown. „Tworzymy liposom, który zawiera cholesterol i mamy nadzieję, że cała lub większość toksyny zwiąże się z liposomem zamiast z komórkami gospodarza” – dodaje, tłumacząc również, że gdy toksyna zwiąże się z liposomem, powinna prowadzić do uwolnienia antybiotyków, zabijając w ten sposób chorobotwórcze bakterie.
Dr Brown uważa, że stosowanie kontrolowanego systemu dostarczania antybiotyków może pomóc w leczeniu nie tylko agresywnego zapalenia przyzębia, ale także innych chorób. „Ponieważ toksyna, nad którą pracujemy jest blisko spokrewniona z tymi, które powodują choroby, takie jak krztusiec, cholera i infekcje E. coli, to podejście takie może być przydatne w walce przeciwko wielu bakteriom” – podsumowała.
Dane pochodzą z informacji o projekcie badawczym pt.: „Kontrolowane podłoże do podawania antybiotyków w leczeniu agresywnego zapalenia przyzębia” („Controlled antibiotic delivery vehicle for treatment of aggressive periodontitis”).
Ostatnie badania pokazujące wzrost liczby pacjentów z zapaleniem przyzębia, a także badania łączące ten stan z chorobą Alzheimera doprowadziły do ...
W czasie tegorocznego kongresu „Europerio”, który odbył się w Wiedniu, firma Heraeus przeprowadziła sympozja dotyczące najnowszych ...
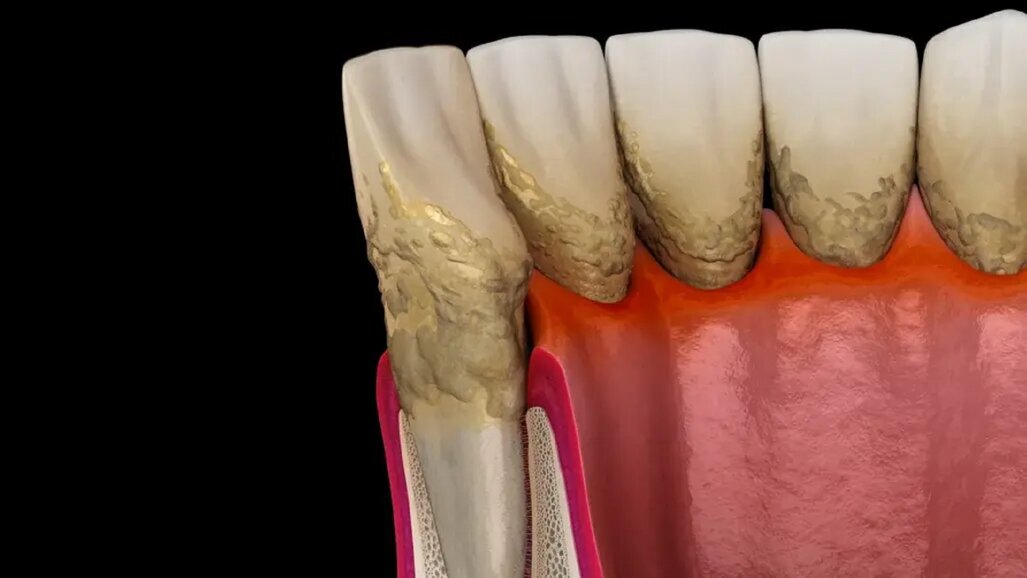
Zapalenie przyzębia oznacza zniszczenie więzadła ozębnowego oraz podparcia kostnego na skutek działania stanu zapalnego. Przebieg tej choroby ...
Zapalenie przyzębia oznacza zniszczenie więzadła ozębnowego oraz podparcia kostnego na skutek działania stanu zapalnego. Przebieg tej choroby ...
Nowe podejście do leczenia zapalenia przyzębia może sprawić, że stosowanie antybiotyków stanie się przestarzałe, ponieważ atakuje tylko bakterie ...
BRUKSELA, Belgia: Biorąc pod uwagę częstość występowania i profilaktykę dot. zapalenia przyzębia, Europejska Federacja Periodontologii (EFP) uważa,...
U pacjentów z nieswoistymi zapaleniami jelit zaobserwowano blisko 3,5- krotnie większe ryzyko chorób przyzębia o średnim lub dużym nasileniu (fot.: ...
FILADELFIA, USA: Zapalenie przyzębia to jedna z najpowszechniejszych chorób na świecie, dotykająca od 20% do 50% populacji, czyli około 64 milionów ...
Większość dorosłych doświadcza epizodów zapalenia dziąseł, które mogą przejść w zapalenie przyzębia, jednak rola płytki nazębnej w ...
W badaniu poddano analizie związek między udarem mózgu a zapaleniem przyzębia, jednej z najczęstszych chorób, dotykającej ponad 700 mln ludzi na ...
SÃO PAULO, Brazylia: Medycyna naturalna i metody leczenia z wykorzystaniem związków pochodzenia roślinnego cieszą się coraz większym ...
Webinarium na żywo
pon. 1 czerwca 2026
7:00 (CET) Warsaw
Webinarium na żywo
śro. 3 czerwca 2026
7:00 (CET) Warsaw
Webinarium na żywo
czw. 4 czerwca 2026
8:00 (CET) Warsaw
Webinarium na żywo
pon. 8 czerwca 2026
6:00 (CET) Warsaw
Webinarium na żywo
pon. 8 czerwca 2026
7:00 (CET) Warsaw
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Webinarium na żywo
pon. 8 czerwca 2026
8:00 (CET) Warsaw
Webinarium na żywo
śro. 10 czerwca 2026
5:00 (CET) Warsaw



 Austria / Österreich
Austria / Österreich
 Bośnia i Hercegowina / Босна и Херцеговина
Bośnia i Hercegowina / Босна и Херцеговина
 Bułgaria / България
Bułgaria / България
 Chorwacja / Hrvatska
Chorwacja / Hrvatska
 Czechy i Słowacja / Česká republika & Slovensko
Czechy i Słowacja / Česká republika & Slovensko
 Francja / France
Francja / France
 Niemcy / Deutschland
Niemcy / Deutschland
 Grecja / ΕΛΛΑΔΑ
Grecja / ΕΛΛΑΔΑ
 Węgry / Hungary
Węgry / Hungary
 Włochy / Italia
Włochy / Italia
 Holandia / Nederland
Holandia / Nederland
 nordycki / Nordic
nordycki / Nordic
 Polska / Polska
Polska / Polska
 Portugalia / Portugal
Portugalia / Portugal
 Rumunia i Mołdawia / România & Moldova
Rumunia i Mołdawia / România & Moldova
 Słowenia / Slovenija
Słowenia / Slovenija
 Serbia i Czarnogóra / Србија и Црна Гора
Serbia i Czarnogóra / Србија и Црна Гора
 Hiszpania / España
Hiszpania / España
 Szwajcaria / Schweiz
Szwajcaria / Schweiz
 indyk / Türkiye
indyk / Türkiye
 Wielka Brytania i Irlandia / UK & Ireland
Wielka Brytania i Irlandia / UK & Ireland
 Międzynarodowy / International
Międzynarodowy / International
 Brazylia / Brasil
Brazylia / Brasil
 Kanada / Canada
Kanada / Canada
 Ameryka Łacińska / Latinoamérica
Ameryka Łacińska / Latinoamérica
 USA / USA
USA / USA
 Chiny / 中国
Chiny / 中国
 Indie / भारत गणराज्य
Indie / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Wietnam / Việt Nam
Wietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Izrael / מְדִינַת יִשְׂרָאֵל
Izrael / מְדִינַת יִשְׂרָאֵל
 Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
 Bliski Wschód / Middle East
Bliski Wschód / Middle East









































To post a reply please login or register