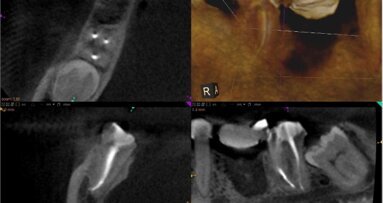
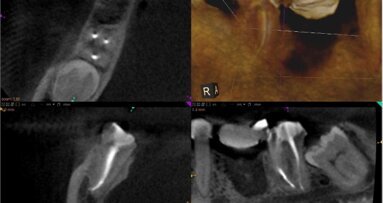
Wskaźnik powodzenia leczenia endodontycznego waha się w zakresie 85-97%. Dla uzyskania takiego poziomu niezbędne są: stosowanie właściwych protokołów terapeutycznych, wiedza oraz kontrola infekcji (Ryc. 1a-d).
Infekcja endodontyczna
Wiadomo, że zmiany w obrębie przyzębia wierzchołkowego wywołane są przez przechodzenie mikroorganizmów bytujących w kanałach i ich produktów do otaczających tkanek przyzębia. Ekspozycja miazgi zęba na środowisko jamy ustnej – czy to bezpośrednio, czy też przez kanały dodatkowe, otwarte kanaliki zębinowe lub kieszonki periodontologiczne – to najbardziej prawdopodobna droga infekcji endodontycznej.
Klinicznie zapalenie przyzębia wierzchołkowego nie jest zauważalne do czasu, kiedy dojdzie do zakażenia tkanki martwiczej drobnoustrojami. Wyizolowano do 40 gatunków bakterii obecnych w kanałach korzeniowych. W przypadku infekcji pierwotnej często rozpoznaje się ziarniaki, pałeczki, bakterie nitkowate, krętki, bakterie beztlenowe i względnie beztlenowe. Można także wyizolować grzyby. Drobnoustroje endodontyczne można znaleźć zawieszone w głównym kanale korzeniowym, przyczepione do ścian kanału oraz ukryte głęboko w kanalikach zębinowych na głębokości do 300 μm (Ryc. 2a-c). Brak cementu znacznie zwiększa penetrację kanalików zębinowych przez bakterie.
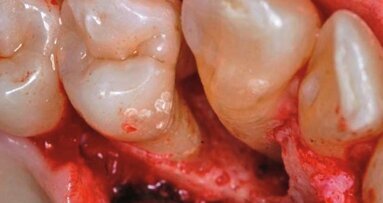
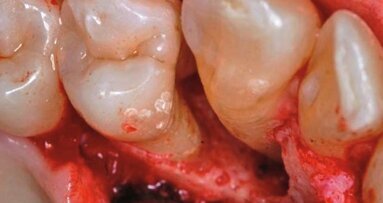
Wykazano, że bakterie można znaleźć także poza systemem kanałów korzeniowych, w obrębie cementu korzeniowego albo w postaci biofilmu na zewnętrznej powierzchni wierzchołka. W przypadku konwencjonalnego leczenia endodontycznego zębów ze zmianami okołowierzchołkowymi ok. 15-20% przypadków kończy się niepowodzeniem. Przyczyną jest obecność bakterii po odkażeniu lub brak możliwości szczelnego zamknięcia kanałów na zakończenie leczenia. Utrzymujące się zakażenie zębów leczonych endodontycznie powoduje podtrzymywanie patologicznych zmian w tkankach wierzchołkowych.
W przypadku niepowodzenia leczenia endodontycznego pierwszy wybór stanowi rewizja tego leczenia. Drobnoustroje obecne w ogniskach utrzymującego się zakażenia różnią się w stosunku do infekcji pierwotnych (Ryc. 3a-c). Często występują względnie beztlenowe bakterie Gram-dodatnie (G+) i Gram-ujemne (G-) oraz grzyby. Szczególną uwagę zwraca się na Enterococcus faecalis, oporną, względnie beztlenową bakterię z grupy G+ ziarniaków, rozpoznawaną znacznie częściej w obrębie kanałów w przypadkach niepowodzenia leczenia endodontycznego. Kontrola infekcji bakteryjnej ma istotne znaczenie dla powodzenia leczenia endodontycznego. Niezbędna jest odpowiednia, skuteczna dezynfekcja systemu kanałów korzeniowych.
embedImagecenter("Imagecenter_1_575",575, "large");
Leczenie endodontyczne
Flora bakteryjna obecna w kanałach korzeniowych musi być wyeliminowana w aktywny sposób, poprzez połączenie oczyszczania mechanicznego i przeciwbakteryjnej terapii chemicznej. Opracowanie mechaniczne prowadzi do eliminacji ponad 90% drobnoustrojów. Ważne jest nadanie kanałowi prawidłowego kształtu. Oceniając skuteczność eliminacji bakterii po samej tylko preparacji mechanicznej, Dalton i wsp. stwierdzili, że opracowanie do rozmiaru 25 w okolicy wierzchołka pozwalało uzyskać negatywny wynik hodowli bakteryjnej w 20% kanałów. Po opracowaniu do rozmiaru 35 wynik negatywny uzyskano w 60% przypadków.
Płyny do płukania stosuje się jako uzupełnienie preparacji mechanicznej w celu zwiększenia wydajności skrawania, usuwania resztek i warstwy mazistej, rozpuszczenia macierzy organicznej, oczyszczenia miejsc niedostępnych dla narzędzi oraz działania przeciwbakteryjnego. Płynem najczęściej stosowanym do płukania kanałów korzeniowych jest podchloryn sodu. Charakteryzuje się on doskonałymi zdolnościami oczyszczania, rozpuszcza tkanki martwicze, ma potencjalne działanie przeciwbakteryjne i – w zależności od stężenia – jest dobrze tolerowany przez tkanki biologiczne. W połączeniu z preparacją mechaniczną redukuje liczbę zakażonych kanałów o 40-50%.
Podczas opracowywania kanałów stosuje się także inne płyny do płukania. EDTA to związek chelatujący, stosowany głównie w celu usuwania warstwy mazistej i ułatwienia usuwania resztek z kanału, nie ma natomiast działania przeciwbakteryjnego. Glukonian chlorheksydyny wywiera silne działanie przeciwbakteryjne wobec dużej liczby gatunków bakteryjnych, nawet opornego E. faecalis, ale nie niszczy białek i martwiczych tkanek tak, jak podchloryn sodu.
Ponieważ preparacja mechaniczna i płukanie nie są w stanie całkowicie wyeliminować bakterii z systemu kanałów korzeniowych, co jest niezbędne dla wypełnienia kanałów, badano wykorzystanie innych substancji i leków jako uzupełnienia standardowego protokołu leczenia endodontycznego. Podstawowym celem opatrunków wprowadzanych do kanału pomiędzy kolejnymi wizytami jest zapewnienie bezpiecznego działania przeciwbakteryjnego o długotrwałej skuteczności.Jako materiał opatrunkowy stosowano wiele różnych związków, takich jak formokrezol, kamforowany parachlorofenol, eugenol, roztwór jodu w jodku potasu, antybiotyki, wodorotlenek wapnia i chlorheksydyna.
Wodorotlenek wapnia stosuje się w leczeniu endodontycznym od 1920 r. Dzięki wysokiej wartości pH (powyżej 11) indukuje on mineralizację, redukuje liczbę bakterii i rozpuszcza tkanki. Dla uzyskania przedłużonego działania przeciwbakteryjnego konieczne jest utrzymywanie wysokiego pH w kanale oraz w zębinie. Utrzymanie pH zależy od dyfuzji przez kanaliki zębinowe.
Chociaż większość mikroorganizmów ginie w pH 9,5, nieliczne mogą przetrwać pH 11 lub nawet wyższe, np. E. faecalis i Candida. Ze względu na oporność niektórych mikroorganizmów na konwencjonalne protokoły terapeutyczne oraz bezpośrednią zależność pomiędzy obecnością żywych bakterii w systemie kanałów korzeniowych a gorszym wskaźnikiem powodzenia leczenia, podejmowane są nowe działania, mające na celu kontrolę infekcji kanałów.
Lasery w endodoncji
Lasery wprowadzono do endodoncji jako terapię uzupełniającą konwencjonalne leczenie przeciwbakteryjne. Działanie przeciwbakteryjne lasera Nd:YAG, diodowego, Er-YAG oraz dezynfekcji przez fotoaktywację badało wielu naukowców. W dalszej części niniejszego artykułu opisano każdy z laserów, aby ułatwić wybór odpowiedniego protokołu postępowania, zapewniającego duże prawdopodobieństwo skutecznego leczenia zębów z zapaleniem przyzębia wierzchołkowego.
Laser Nd:YAG
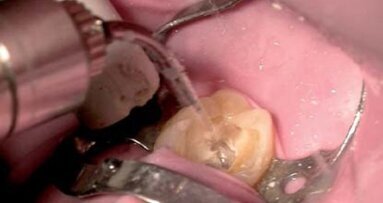
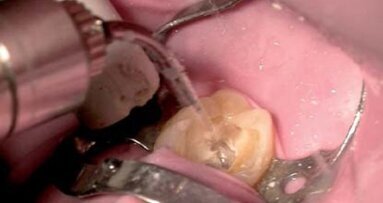
Był to jeden z pierwszych laserów badanych pod kątem zastosowania w endodoncji. Jest to laser na ciele stałym. Medium aktywnym jest zwykle granat itrowo-glinowy (Y3Al5O12), w którym niektóre z jonów Y3+ zostały zastąpione jonami Nd3+. Jest to system o 4 poziomach energii, działający w trybie fali ciągłej lub trybie pulsacyjnym. Emituje światło podczerwone o długości fali 1064 nm. W związku z tym do wykorzystania klinicznego niezbędny jest światłowód. W tym celu stosuje się elastyczne światłowody o średnicy 200-400 μm. Laser można stosować na wewnętrznej powierzchni kanału korzeniowego w trybie kontaktowym (Ryc. 4a, b). Na typowej ścianie kanału korzeniowego po zastosowaniu lasera Nd:YAG widoczna jest stopiona zębina o sferycznym, szklistym wyglądzie. Nieliczne miejsca pokryte są warstwą mazistą. W niektórych miejscach widoczne są kanaliki zębinowe szczelnie zamknięte zębiną stopioną ze złogami mineralnymi. Ta modyfikacja morfologiczna znacząco zmniejsza przepuszczalność zębiny, jednak ponieważ wiązka laserowa jest emitowana ze światłowodu wzdłuż kanału korzeniowego, a nie w kierunku bocznym, ściany kanału nie są napromieniowane na całej powierzchni, co zapewnia skuteczniejsze działanie w części wierzchołkowej kanału. Niepożądane zmiany morfologiczne, takie jak zwęglenie i pękanie są widoczne tylko w przypadku użycia wysokich ustawień energii. Jednym z głównych problemów dotyczących wewnątrzkanałowego stosowania promieniowania laserowego jest wzrost temperatury na powierzchni zewnętrznej korzenia. Działając na tkanki, światło lasera wywiera efekt termiczny. Wzrost temperatury jest bezpośrednio związany ze stosowaną energią, czasem i trybem naświetlania. Wzrost temperatury przekraczający 10° C/min. może prowadzić do uszkodzenia tkanek przyzębia, ich martwicy i ankylozy.
Lan 38 badał w warunkach in vitro wzrost temperatury na powierzchni zewnętrznej korzenia po zastosowaniu lasera Nd:YAG przy następujących ustawieniach energii: 50, 80 i 100 mJ przy 10, 20 i 30 impulsach/s. Wzrost temperatury nie przekraczał 10° C. Takie same wyniki uzyskali Bachman i wsp., Kimura i wsp. oraz Gutknecht i wsp. W przeciwieństwie do powierzchni zewnętrznej, temperatura wewnątrz kanału dramatycznie rośnie w części wierzchołkowej, co skutecznie chroni przed skażeniem przez bakterie. W przypadku lasera Nd:YAG bezpieczne ustawienia energii z punktu widzenia temperatury i zmian morfologicznych to 1,5 W i 15 Hz .
Zastosowanie lasera Nd:YAG w endodoncji jest przede wszystkim ukierunkowane na eliminację mikroorganizmów z systemu kanałów korzeniowych. Rooneyi wsp. oceniali działanie przeciwbakteryjne lasera Nd:YAG w warunkach in vitro. Uzyskano redukcję liczby bakterii przy uwzględnieniu parametrów ustawień energii. Naukowcy opracowali różne modele in vitro, symulujące obecność mikroorganizmów, których można spodziewać się w martwych, skażonych zębach. Promieniowanie lasera Nd:YAG skutecznie działało na bakterie z gatunków Bacillus stearothermophilus, Streptococcus faecalis, Escherichia coli, Streptococcus mutans, Streptococcus sanguis, Prevotella intermedia oraz na typowe drobnoustroje oporne na konwencjonalne leczenie endodontyczne, E. faecalis. Laser Nd:YAG wywiera na zębinę działanie przeciwbakteryjne na głębokości 1000 μm (Ryc. 5).
Opracowano także modele histologiczne w celu oceny reakcji tkanek okołowierzchołkowych po wewnątrzkanałowym zastosowaniu lasera Nd:YAG. Suda i wsp. wykazali w badaniach na psach, że zastosowanie lasera Nd:YAG przy ustawieniach 100 mJ/30 impulsów/s przez 30 s jest bezpieczne dla tkanek otaczających korzeń. Maresca i wsp. potwierdzili na zębach ludzkich przeznaczonych do resekcji wierzchołka wyniki uzyskane przez Suda i wsp. oraz Ianamoto i wsp. Koba i wsp. analizowali zapalną reakcję histopatologiczną po zastosowaniu u psów lasera Nd:YAG przy 1 i 2 W. Wyniki wykazały znaczącą redukcję stanu zapalnego po 4 i 8 tygodniach w porównaniu do grupy, w której nie stosowano napromieniowania.
Opublikowane w piśmiennictwie raporty kliniczne potwierdzają korzyści wynikające z wewnątrzkanałowego stosowania laserów Nd:YAG. W r. 1993 Eduardo i wsp. opisali przypadek skutecznego, złożonego leczenia endodontycznego z użyciem promieniowania lasera Nd:YAG w celu rewizji leczenia kanałowego, leczenia zapalenia tkanek okołowierzchołkowych, ostrego ropnia i perforacji. Kontrola kliniczna i radiologiczna wykazała całkowite wygojenie po 6 miesiącach. Podobne wyniki uzyskali Camargo i wsp. Gutknecht i wsp. opisali znaczącą poprawę przebiegu gojenia leczonych laserowo zakażonych kanałów w porównaniu do leczenia bez napromieniowania. Camargo i wsp. porównali w warunkach in vivo efekt przeciwbakteryjny tradycyjnego leczenia endodontycznego i konwencjonalnego protokołu z użyciem lasera Nd:YAG. Badaniem objęto zęby z przejaśnieniem okołowierzchołkowym i martwą miazgą, bez dolegliwości klinicznych, które podzielono na 2 grupy, poddane leczeniu tradycyjnemu i leczeniu z napromieniowaniem laserem. Pobierano próbki do badania mikrobiologicznego przed preparacją kanału, po preparacji i/lub napromieniowaniu oraz po 7 dniach od leczenia. Wyniki wykazały znaczący efekt przeciwbakteryjny w grupie leczonej laserem w porównaniu do konwencjonalnej terapii. Ponieważ nie stosowano żadnych innych środków przeciwbakteryjnych, uznano, że to laser Nd:YAG odgrywał istotną rolę w redukcji liczby bakterii podczas leczenia endodontycznego.
Lasery diodowe
Laser diodowy to półprzewodnikowy laser na ciele stałym, który jako medium aktywne wykorzystuje kombinację galu, arsenku, glinu i/lub indu. Długości fali dostępne dla zastosowań stomatologicznych należą do przedziału 800-1064 nm. Laser emituje falę ciągłą lub bramkowane impulsy. Promieniowanie jest dostarczane za pośrednictwem światłowodu (Ryc. 6a, b). Lasery diodowe wzbudzają rosnące zainteresowanie wśród lekarzy dentystów ze względu na ich niewielkie rozmiary i przystępną cenę. Do zalet tego lasera należą: eliminacja warstwy mazistej, redukcja liczby bakterii i zmniejszony przeciek wierzchołkowy. Dzięki nim laser diodowy nadaje się do stosowania w ramach leczenia endodontycznego. Działanie lasera opiera się przede wszystkim na reakcji fototermicznej. Efekt termiczny w obrębie tkanek zależy od trybu i ustawień promieniowania. Wang i wsp. naświetlali kanały korzeniowe w warunkach in vitro z mocą 5 W przez 7 s i wykazali wzrost temperatury, który nie przekroczył 8,1° C. Podobne wyniki uzyskał Da Costa Ribeiro. Gutknecht i wsp. oceniali stosowanie lasera diodowego wewnątrz kanałów przy mocy wyjściowej 1,5 W i stwierdzili wzrost temperatury na powierzchni zewnętrznej korzenia o 7° C. Laser diodowy emitujący falę o długości 980 nm przy ustawieniach mocy 2,5 W w trybie ciągłym lub przerywanym nigdy nie powodował wzrostu temperatury powyżej 47° C, która jest uważana za bezpieczną dla tkanek przyzębia.
Zmiany morfologiczne obserwowane w części wierzchołkowej kanału po naświetleniu laserem diodowym obejmowały czystą powierzchnię zębiny wewnątrzkanałowej ze szczelnie zamkniętymi kanalikami korzeniowymi, wskazującymi na stopienie i ponowną krystalizację. Zasadniczo długości fali bliskie podczerwieni, takie jak 1064 i 980 nm, sprzyjają fuzji i ponownej krystalizacji powierzchni zębiny, co powoduje szczelne zamknięcie kanalików zębinowych.
Oczywistą konsekwencją jest fakt, że promieniowanie lasera diodowego wywiera potencjalny efekt przeciwbakteryjny. W większości przypadków działanie to ma bezpośredni związek z ilością dostarczonej energii. Gutknecht i wsp. przeprowadzili badanie porównawcze stwierdzając, że laser diodowy 810 nm stosowany w trybie fali ciągłej z mocą wyjściową 0,6 W umożliwiał redukcję skażenia bakteryjnego nawet o 88,38%. Laser diodowy 980 nm miał znaczące działanie przeciwbakteryjne średnio w obrębie 77-97% kanałów korzeniowych skażonych E. faecalis. Badano energię wyjściową równą 1,7; 2,3 oraz 2,8 W. Skuteczność była bezpośrednio związana z ilością energii i grubością zębiny.
Laser Er:YAG
Są to lasery na ciele stałym, w których źródłem promieniowania jest domieszkowany erbem granat itrowo-glinowy (Er:Y3Al5O12). Lasery Er:YAG zwykle emitują fale o długości 2940 nm, co odpowiada podczerwieni. W przeciwieństwie do laserów Nd:YAG, promieniowanie emitowane przez laser Er:YAG jest w znacznym stopniu pochłaniane przez wodę ze względu na rezonans na poziomie atomowym. Fale emitowane przez laser Er:YAG są dobrze absorbowane przez tkanki twarde zęba. Laser ten został dopuszczony do stosowania w stomatologii w 1997 r. Wskazania do jego stosowania w leczeniu endodontycznym obejmują usuwanie warstwy mazistej, preparację kanału i resekcję wierzchołka korzenia (Ryc. 7).
Morfologicznie zębina poddana naświetlaniu laserem Er:YAG charakteryzuje się czystymi obszarami z otwartymi kanalikami zębinowymi i wolnymi od warstwy mazistej w obrębie sferycznej powierzchni. Moritz i wsp. obserwowali redukcję liczby bakterii związaną ze stosowaniem lasera Er:YAG. Stabholz i wsp. opisują nową końcówkę endodontyczną, którą można stosować wraz z systemem lasera Er:YAG. Końcówka ta zamiast bezpośredniej emisji umożliwia emisję boczną promieniowania dzięki pojedynczemu otworkowi umieszczonemu na dalekim końcu. Światło jest emitowane przez spiralne włókno, umieszczone wzdłuż końcówki. Stabholz i wsp. oceniali skuteczność spiralnej końcówki w usuwaniu warstwy mazistej. Stwierdzili, że ściany zębiny kanałowej w badaniu mikroskopem skaningowym były czyste, wolne od warstwy mazistej i resztek.
Dezynfekcja aktywowana światłem (PAD)
PAD (photoactivated disinfection) to inna metoda odkażania stosowana w endodoncji, wykorzystująca fakt, że substancje aktywowane przez światło o określonej długości fali wiążą się z komórkami docelowymi. Powstają wolne rodniki, które wywierają działanie toksyczne w stosunku do bakterii. Przykład substancji ulegających fotoaktywacji stanowią błękit toluidynowy i błękit metylenowy. Błękit toluidynowy zabija większość bakterii w jamie ustnej. W badaniach in vitro wykazano skuteczne działanie terapii PAD na wrażliwe bakterie, takie jak E. faecalis, Fusobacterium nucleatum, P. intermedia, Peptostreptococcus micros i Actinomycetemcomitans. Z kolei Souza i wsp. w badaniu mającym na celu ocenę efektu przeciwbakteryjnego terapii PAD, stosowanej jako uzupełnienie preparacji/płukania kanałów zakażonych E. faecalis, nie wykazali znaczącego wpływu na dezynfekcję światła kanałów. Być może dalszy rozwój protokołów PAD i badania porównawcze umożliwią opracowanie zaleceń dotyczących ich stosowania klinicznego.
Omówienie i wnioski
W leczeniu martwych, skażonych zębów warto jest skupić się na zniszczeniu bakterii obecnych w kanale korzeniowym. Szanse na korzystny efekt leczenia są znacząco wyższe, jeśli na etapie wypełniania kanału jest on wolny od bakterii. Jeśli jednak podczas wypełniania kanału pozostaną w nim bakterie, zwiększa się ryzyko niepowodzenia leczenia. Dlatego podstawowym celem terapii jest uzyskanie całkowitej eliminacji bakterii z systemu kanałów korzeniowych.
Obecnie dobrze znane jest potencjalne przeciwbakteryjne działanie promieniowania laserowego w połączeniu z efektem biostymulacyjnym i przyspieszeniem procesów gojenia. Badania potwierdzają zasadność udoskonalania protokołu leczenia endodontycznego. Terapia laserowa w toku leczenia endodontycznego ma w porównaniu do konwencjonalnego leczenia pewne zalety, takie jak minimalny przeciek wierzchołkowy, skuteczne zwalczanie opornych mikroorganizmów i zewnętrznego biofilmu okołowierzchołkowego. Z tego względu konwencjonalne leczenie wzbogacono o zabiegi z użyciem lasera w celu poprawy efektów terapii endodontycznej (Ryc. 8 a-d).
Badania kliniczne wykazały zalety stosowania lasera w leczeniu endodontycznym w przypadkach zapalenia tkanek okołowierzchołkowych. Protokół leczenia endodontycznego obejmuje oczyszczenie i poszerzenie kanału korzeniowego co najmniej do rozmiaru ISO 35, stosowanie płynów do płukania o działaniu przeciwbakteryjnym i naświetlanie kanału korzeniowego przy użyciu kontrolowanej wielkości energii. Dla uzyskania optymalnych efektów konieczne jest idealnie szczelne wypełnienie kanału i prawidłowa odbudowa korony zęba.
W praktyce zastosowanie lasera wymaga niewiele więcej czasu. Naświetlanie jest proste, jeśli stosuje się elastyczne światłowody o średnicy 200 μm. Światłowód bez trudu dociera do wierzchołkowej 1/3 kanału, nawet w przypadku zakrzywionych korzeni zębów trzonowych (Ryc. 9). Energia emitowana przez laser działa na warstwę zębinową, a także na rejon okołowierzchołkowy, poza wierzchołkiem korzenia. Laser działa nawet na niedostępne okolice, np. biofilm pokrywający od zewnątrz wierzchołek korzenia.
Podczas naświetlania należy przestrzegać podstawowych zasad. Kanał korzeniowy musi być wilgotny. Należy wykonywać ruch obrotowy, przesuwając z się okolicy dokoronowej w stronę wierzchołka. Należy też utrzymywać kontakt ze ścianami kanału (Ryc. 10 a-c). Ustawienia energii i tryb naświetlania zależą od wyboru określonej długości fali.
Lasery Nd:YAG, diodowe (o różnej długości fali), Er:YAG oraz lasery niskiej mocy można stosować podczas różnych zabiegów, uzyskując akceptowalne wyniki. Wykorzystanie technologii laserowej w stomatologii jest faktem. Opracowanie specjalnych światłowodów i ewolucja laserów w połączeniu z coraz lepszym rozumieniem interakcji pomiędzy laserem i tkankami prowadzą do lepszych możliwości i poszerzenia wskazań do ich stosowania w leczeniu endodontycznym.
Piśmiennictwo dostępne u wydawcy.
Kontakt:
Dr Selma Camargo
University of São Paulo
Rua Pinto Gonçalves, 85/54 Perdizes
São Paulo, SP 05005-010, Brazylia
E-mail: selmacris@me.com
Najczęstszą przyczyną niepowodzenia leczenia implantoprotetycznego jest periimplantitis. Wśród niechirurgicznych metod leczenia tego schorzenia ...
Celem niniejszego artykułu jest przedstawienie przydatności badania tomograficznego wiązki stożkowej w ocenie anatomii oraz jakości wypełnienia ...
Celem niniejszego artykułu jest przedstawienie przydatności badania tomograficznego wiązki stożkowej w ocenie anatomii oraz jakości wypełnienia ...
Sukces usunięcia miazgi zęba w dużej mierze zależy od eliminacji bakterii z kanału korzeniowego. Naukowcy eksperymentowali z nową mieszanką ...
Podejście do pacjenta w stomatologii dziecięcej wymaga bliskiej współpracy pomiędzy dentystami a rodzicami oraz samymi dziećmi. Terapia laserowa...
Podejście do pacjenta w stomatologii dziecięcej wymaga bliskiej współpracy pomiędzy dentystami a rodzicami oraz samymi dziećmi. Terapia laserowa...
W ciągu ostatnich 10 lat dobrze udokumentowano wykorzystanie laserów w leczeniu periodontologicznym. Lasery mogą być wykorzystywane podczas ...
W ciągu ostatnich 10 lat dobrze udokumentowano wykorzystanie laserów w leczeniu periodontologicznym. Lasery mogą być wykorzystywane podczas ...
O fenomenie witaminy D mówi i pisze się dużo, ale temat należy nieustannie przypominać i do tego tematu wracać. Dotychczas powstało wiele prac ...
Nowotwory jamy ustnej stanowią poważny odsetek wszystkich zachorowań na raka. Nowa terapia genowa może dać nadzieję na zwiększenie powodzenia ...
Webinarium na żywo
wto. 19 maja 2026
5:00 (CET) Warsaw
Webinarium na żywo
wto. 19 maja 2026
7:00 (CET) Warsaw
Prof. Dr. med. dent. Ivo Krejci
Webinarium na żywo
śro. 20 maja 2026
1:00 (CET) Warsaw
Dr. Graham Carmichael BDSc (Hons), DClinDent (Pros), FRACDS, Dr. Robert Gottlander DDS
Webinarium na żywo
śro. 20 maja 2026
3:00 (CET) Warsaw
Webinarium na żywo
śro. 20 maja 2026
5:00 (CET) Warsaw
Webinarium na żywo
śro. 20 maja 2026
7:00 (CET) Warsaw
Prof. Dr. med. dent. Tim Joda PhD, MSc, eMBA
Webinarium na żywo
czw. 21 maja 2026
6:00 (CET) Warsaw
Dr. Leonardo Muniz DDS, MSC



 Austria / Österreich
Austria / Österreich
 Bośnia i Hercegowina / Босна и Херцеговина
Bośnia i Hercegowina / Босна и Херцеговина
 Bułgaria / България
Bułgaria / България
 Chorwacja / Hrvatska
Chorwacja / Hrvatska
 Czechy i Słowacja / Česká republika & Slovensko
Czechy i Słowacja / Česká republika & Slovensko
 Francja / France
Francja / France
 Niemcy / Deutschland
Niemcy / Deutschland
 Grecja / ΕΛΛΑΔΑ
Grecja / ΕΛΛΑΔΑ
 Węgry / Hungary
Węgry / Hungary
 Włochy / Italia
Włochy / Italia
 Holandia / Nederland
Holandia / Nederland
 nordycki / Nordic
nordycki / Nordic
 Polska / Polska
Polska / Polska
 Portugalia / Portugal
Portugalia / Portugal
 Rumunia i Mołdawia / România & Moldova
Rumunia i Mołdawia / România & Moldova
 Słowenia / Slovenija
Słowenia / Slovenija
 Serbia i Czarnogóra / Србија и Црна Гора
Serbia i Czarnogóra / Србија и Црна Гора
 Hiszpania / España
Hiszpania / España
 Szwajcaria / Schweiz
Szwajcaria / Schweiz
 indyk / Türkiye
indyk / Türkiye
 Wielka Brytania i Irlandia / UK & Ireland
Wielka Brytania i Irlandia / UK & Ireland
 Międzynarodowy / International
Międzynarodowy / International
 Brazylia / Brasil
Brazylia / Brasil
 Kanada / Canada
Kanada / Canada
 Ameryka Łacińska / Latinoamérica
Ameryka Łacińska / Latinoamérica
 USA / USA
USA / USA
 Chiny / 中国
Chiny / 中国
 Indie / भारत गणराज्य
Indie / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Wietnam / Việt Nam
Wietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Izrael / מְדִינַת יִשְׂרָאֵל
Izrael / מְדִינַת יִשְׂרָאֵל
 Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
 Bliski Wschód / Middle East
Bliski Wschód / Middle East














































To post a reply please login or register