Najczęstszą przyczyną niepowodzenia leczenia implantoprotetycznego jest periimplantitis. Wśród niechirurgicznych metod leczenia tego schorzenia dużą popularność zyskały lasery o technologii bezkontaktowej: Er:YAG, diodowy i CO2. Charakteryzują się one dużą zdolnością dekontaminacji powierzchni wszczepu i tkanek okołowszczepowych, a także możliwością zwiększenia ich potencjału regeneracyjnego, nie uszkadzając przy tym powierzchni implantu.
Periimplantitis jest głównym czynnikiem sprawczym niepowodzenia leczenia implantoprotetycznego. Do tej pory przedstawiono wiele różnych metod zapobiegania i leczenia tego stanu chorobowego. W postępowaniu klinicznym dzielimy je na metody chirurgiczne i niechirurgiczne. Do chirurgicznych metod leczenia periimplantitis należą resekcja zapalnie zmienionych tkanek, mechaniczne oczyszczanie i wygładzanie powierzchni wszczepu, stosowanie materiałów kościozastępczych i błon zaporowych. Coraz większym zainteresowaniem cieszą się również lasery, które można wykorzystać do scalingu, cięcia, usuwania zapalnie zmienionych tkanek i remodelowania kości.1 Należy podkreślić, że preferowane są metody niewpływające na porowatość powierzchni. Wiąże się to z zachowaniem struktury warstw tlenku tytanu i wolnej energii powierzchni materiału.2
W przeciwieństwie do mechanicznie przygotowanych oraz gładkich powierzchni implantu, powierzchnie porowate wykazują lepsze połączenie z kością i osteointegrację.3 Właściwości powierzchni, zwłaszcza hydrofilność i szorstkość mają znaczący wpływ na adhezję, proliferację, zmiany morfologiczne i zmiany w funkcjonowaniu komórek.2 Jednoczesna utrata przyczepu tkanek twardych i miękkich wokół implantu powoduje ekspozycję porowatej powierzchni implantu na kolonizację bakterii. Wysokie powinowactwo mikroorganizmów do obnażonej powierzchni wszczepu uniemożliwia niejednokrotnie efektywne fizjologiczne i mechaniczne oczyszczanie poprzez przepływ śliny i higienę. Wówczas rozwój zapalenia błony śluzowej i periimplantitis są często nieuniknione.4
Tkanki miękkie otaczające implant czynnościowo imitują tkanki przyzębia brzeżnego. Oba rodzaje tych struktur posiadają także podobieństwa anatomofizjologiczne. Pomiędzy wszczepem a dziąsłem stwierdza się obecność przyczepu nabłonkowego o długości oscylującej wokół wartości 1,5 mm, nabłonek łączący rozciąga się na długość 2 mm.5 Tkanki znajdujące się w bezpośrednim kontakcie z implantem są znacznie słabiej ukrwione ze względu na specyfikę ich budowy. Brak jest tutaj ozębnej, cementu, a tkanka łączna otaczająca wszczep charakteryzuje się odmiennym układem włókien i mniejszą zawartością fibroblastów.6,21
Specyfika anatomofizjologiczna schorzenia definiuje metody leczenia. Ze względu na powszechne stosowanie laserów w terapii, w niniejszym artykule podjęto się analizy właściwości i parametrów wybranych systemów laserowych.
Zastosowanie systemów laserowych
Ze względu na swoje liczne zalety i możliwości zastosowania, wielką popularność w implantologii zdobyły lasery o technologii bezkontaktowej, dowodząc jednocześnie swojej skuteczności w leczeniu periimplantitis. Oddziaływanie promieniowania laserowego na laser jest zdeterminowane przez strumień energii, stopień absorpcji, przewodnictwo cieplne, pojemność oraz budowę powierzchni materiału. Bezkontaktowa ablacja tkanek w połączeniu ze zmniejszonymi: krwawieniem, obrzękiem, bólem i bliznowaceniem, a także unikalny potencjał eliminacji bakterii patogennych sprawia, że preferowane jest zastosowanie laseroterapii w celu dekontaminacji skażonych powierzchni wszczepu i okolicznych tkanek, zwłaszcza w wieloetapowym leczeniu. Należy jednak pamiętać, że promieniowanie laserów monochromatycznych przy odpowiednich parametrach i właściwościach powierzchni implantu może powodować zmiany w strukturze powierzchni wszczepu.7 Takie samo ryzyko niesie ze sobą praca w trybie pulsacyjnym, co może zaburzać proces gojenia zarówno tkanek miękkich, jak i twardych. Ponadto, wzrost temperatury o 10⁰ C utrzymany przez 60 s wystarczy, aby spowodować nieodwracalną destrukcję kości.
Obecnie najczęściej używanymi laserami są diodowy, CO2 i Er:YAG ze względu na swoje właściwości hemostatyczne, selektywne usuwanie złogów kamienia oraz efekt bakteriobójczy, co zapewnia niemal całkowitą lub w niektórych przypadkach całkowitą eliminację bakterii patogennych z powierzchni tytanowych wszczepów, o ile zostały zastosowane przy odpowiednio dobranych do rodzaju powierzchni parametrach.8 Wykorzystują one długości fal odpowiadające wielkości komórek ludzkich i bakterii. Posiadają zdolność dezynfekcji powierzchni wszczepu nie tylko dzięki destrukcji komórek bakteryjnych, ale też wirusów i grzybów. Tkanki zmienione zapalnie w przebiegu periimplantitis zawierają wodę, pigment i hydroksyapatyty. W leczeniu periimplantitis wykorzystywane są takie długości fal, które mogą zostać przez nie zaabsorbowane. Obecnie wiadomo, że lasery CO2 i erbowe są najłatwiej absorbowane przez wodę, diodowe przez pigment, a erbowe także przez hydroksyapaptyty.9
Laser diodowy
Lasery diodowe, dzięki szerokiemu wachlarzowi zalet, tj. małe rozmiary, zadowalający przedział cenowy i uniwersalność w zastosowaniu cieszą się dużym zainteresowaniem również w implantologii.10 Laser diodowy to instrument nieablacyjny, który może kontaktować bezpośrednio z powierzchnią implantu, nie powodując przy tym jej stopienia, pęknięcia czy formowania szczelin. Jego efekt bakteriobójczy objawia się poprzez inaktywację bakteryjnych endotoksyn. Ponadto, ma właściwości hemostatyczne i nie wywołuje produkcji warstwy mazistej. Miejscowy efekt nieznacznego wzrostu temperatury powoduje obniżenie zdolności do chemicznej adhezji kamienia do implantu. Stymuluje także fibroblasty i osteoblasty, co pobudza produkcję przekaźników RNA, a co za tym idzie – także znacznie zwiększoną produkcję kolagenu podczas gojenia tkanek przyzębia.11
Kreisler et al. dowiedli, że laser diodowy w trybie ciągłej fali może być zastosowany przy wiązce promieniowania 400 nm i mocy 2 W (czas 10 s), a laser CO2 może być użyty z mocą do 2,5 W. Zastosowanie takiego ograniczenia parametrów zapobiega niepożądanemu w laserotapii wzrostowi temperatury.12 Możliwe jest to również poprzez zastosowanie chłodzenia wodnego.10,13 Ponadto, laser diodowy jako jedyny, niezależnie od dobranych parametrów, nie wywołuje żadnych negatywnych zmian na powierzchni wszczepu.14 Badania Tosuna et al. udowodniły, że zastosowanie lasera diodowego (wiązka 320 µm) o mocy 1 W przez 10 s powoduje eliminację bakterii Staphylococcus aureus aż w 97%.8 Co więcej, zastosowanie lasera diodowego w leczeniu periimplantitis ułatwia samo przeprowadzenie zabiegu, gdyż dzięki zachowaniu hemostazy i wytwarzaniu ochronnego skrzepu sprzyja lepszemu gojeniu tkanek.13
Laser CO2
W periodontologii należy unikać użycia lasera CO2 w celu usunięcia kamienia poddziąsłowego, ponieważ powoduje rozpuszczanie i zwęglenie cementu korzeniowego. Wykryto również toksyczne produkty w zwęglonej warstwie (pochodne cyjanków). Nie zaobserwowano morfologicznych zmian na powierzchni implantu.
Kreisler i współpracownicy zaobserwowali, że przy zastosowaniu promieniowania o przepływie energii powyżej 30 J/cm2 dochodzi do stopienia powierzchni wszczepów TPS (titanium plasma sprayed – tytanowe zanurzone uprzednio w osoczu) oraz SLA (sandblasted and acid-etched – wypiaskowane i wytrawione kwasem). Takie uszkodzenie powierzchni HA (hydroxyapatite coated – pokryte hydroksyapatytem) zaobserwowano już przy wartości przepływu energii 15 J/cm2.15 Stubinger nie stwierdza żadnych widocznych nieprawidłowości na powierzchni wszczepu SLA przy zastosowaniu dawek rzędu 47 770 J/cm2.16 Z kolei w badaniach Tosuna potwierdzono całkowitą dekontaminację powierzchni implantu SLA z bakterii S. aureus przy mocy 6 W, częstotliwości 20 Hz i po napromienianiu przez 10 s.8 Ponadto Kreisler podkreśla brak wpływu na osseointegrację i przyczep osteoblastów i uważa laser CO2 za skuteczny i bezpieczny w leczeniu periimplantitis, jednak zwraca uwagę na potencjalne niebezpieczeństwo zwęglenia okolicznych tkanek przy wzroście temperatury powierzchni implantu, która może towarzyszyć użyciu tego lasera.17
Lasery neodymowo-jagowy i Ho:YAG
Wg badan Kreislera i wielu innych badaczy, bez względu na wielkość użytej dawki promieniowania lasery te powodują uszkodzenia na powierzchni implantu, wiec nie znajdują zastosowania w leczeniu periimplantitis.12
Laser Er:YAG
Po raz pierwszy został zastosowany przez Zharikova i jest laserem wykorzystującym źródło promieniowania o stałym stanie skupienia i wykorzystującym długość fali równą 2940 nm, czyli bliską długości fali promieniowania podczerwonego. Zaletą tej długości fali jest zdolność do maksymalnej absorpcji wody – jest ona 15 razy większa niż w przypadku lasera CO2 i ok. 20 000 razy większa niż w przypadku lasera neodymowo-jagowego.18
Ze wszystkich zbadanych laserów laser Er:YAG ma najlepsze właściwości w zakresie zdolności do dekonatminacji powierzchni implantu. Co więcej, nie ma ryzyka uszkodzenia okolicznych tkanek. Przy odpowiednich ustawieniach parametrów nie powoduje również uszkodzenia powierzchni implantu i nie zaburza osseointegracji. Charakteryzuje się wysoką zdolnością do usuwania kamienia, płytki i biofilmu obecnego na powierzchni implantu, niezależnie od powierzchni wszczepu.15,19
W badaniach in vitro pokazano, że laser Er:YAG usuwa bakterie P. gingivalis z powierzchni wypiaskowanych i wytrawionych kwasem implantów i pozwala na osseointegrację. W próbach kontrolnych (bez użycia laseru Er:YAG) nie zaobserwowano osteointegracji. [18].
Dekontaminacja powierzchni implantu z bakterii P. gingivalis przy użyciu lasera Er:YAG umożliwiła większy potencjał proliferacyjny fibroblastów niż w przypadku wszczepów skażonych P. gingivalis, a porównywalny ze sterylnymi wszczepami.20 Stubinger et al. zaobserwowali, że już przy wartościach 300 mJ i 10 Hz (dawka 3,821 J/cm2) dochodzi do nieodwracalnych uszkodzeń powierzchni implantu SLA (przygotowanie powierzchni: piaskowanie, abrazja gruboziarnista i wytrawienie kwasem), natomiast w przypadku powierzchni polerowanej zmiany te obserwuje się dopiero przy 500 mJ i 10Hz (dawka 6,369 J/cm2). Żadnych zmian nie zaobserwowano jednak dla wartości 100 J/10 Hz (dawka 1,273 J/cm2). Dowiedziono tym samym, że wzrost energii promieniowania lasera jest skorelowany z utratą porowatości powierzchni implantu, a jego zastosowanie zmniejsza porowatość co najmniej dwukrotnie.16 W przeciwieństwie do lasera CO2 i diodowego, laser Er:YAG posiada znacznie większą zdolność eliminacji bakterii z powierzchni wszczepu.19 Ponadto, do tej pory nie wykazano negatywnego wpływu na tkanki otaczające. Badania Tosuna et al. wskazują na całkowitą dekontaminację powierzchni implantu SLA z bakterii S. aureus przy zastosowaniu lasera Er:YAG o krótkiej pulsacji, energii 90 mJ, 10 Hz i napromienianiu przez 10 s, natomiast te same parametry lasera o bardzo krótkiej pulsacji powodują dekontaminację w 99%.8
Wnioski
Ze względu na swoje liczne zalety i możliwości zastosowania, wielką popularność w implantologii zdobyły lasery o technologii bezkontaktowej, dowodząc jednocześnie swojej skuteczności w leczeniu periimplantitis. Oddziaływanie promieniowania laserowego na wszczep jest zdeterminowane przez strumień energii, stopień absorpcji, przewodnictwo cieplne, pojemność oraz budowę powierzchni materiału.
Bezkontaktowa ablacja tkanek w połączeniu ze zmniejszonymi krwawieniem, obrzękiem, bólem i bliznowaceniem, a także unikalny potencjał eliminacji bakterii patogennych sprawia, że preferowane jest zastosowanie laseroterapii w celu dekontaminacji skażonych powierzchni wszczepu i okolicznych tkanek, zwłaszcza w leczeniu wieloetapowym. Należy jednak pamiętać, że promieniowanie laserów monochromatycznych przy odpowiednich parametrach i właściwościach powierzchni implantu może powodować zmiany w strukturze powierzchni wszczepu.7 Takie samo ryzyko niesie ze sobą praca w trybie pulsacyjnym, co może zaburzać proces gojenia zarówno tkanek miękkich, jak i twardych. Ponadto, wzrost temperatury o 10⁰ C utrzymany przez 60 s wystarczy, aby spowodować nieodwracalną destrukcję kości.
Lasery Er:YAG, CO2 i diodowy są najczęściej stosowane ze względu na wykorzystywane w nich długości fali, które charakteryzują się praktycznie zerową absorpcją promieniowania przez tlenek tytanu i w ten sposób przeciwdziałają transformacji energii w ciepło.16
Piśmiennictwo dostępne u wydawcy.
Autorzy:
Piotr Wesołowski, Paweł Nieckula, Andrzej Wojtowicz – Zakład Chirurgii Stomatologicznej WUM
Magdalena Płachta, Karolina Siuciak – Studenckie Koło Naukowe przy Zakładzie Chirurgii Stomatologicznej WUM
Kontakt: piotrwesolowski01@gmail.com
Celem niniejszego artykułu jest przedstawienie głównych aspektów związanych z patogenezą, diagnostyką i leczeniem periimplantits. Jest to...
Podejście do pacjenta w stomatologii dziecięcej wymaga bliskiej współpracy pomiędzy dentystami a rodzicami oraz samymi dziećmi. Terapia laserowa...
Podejście do pacjenta w stomatologii dziecięcej wymaga bliskiej współpracy pomiędzy dentystami a rodzicami oraz samymi dziećmi. Terapia laserowa...
Wskaźnik powodzenia leczenia endodontycznego waha się w zakresie 85-97%. Dla uzyskania takiego poziomu niezbędne są: stosowanie właściwych ...
W ciągu ostatnich 10 lat dobrze udokumentowano wykorzystanie laserów w leczeniu periodontologicznym. Lasery mogą być wykorzystywane podczas ...
W ciągu ostatnich 10 lat dobrze udokumentowano wykorzystanie laserów w leczeniu periodontologicznym. Lasery mogą być wykorzystywane podczas ...
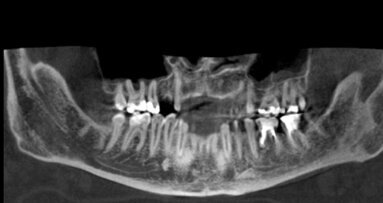
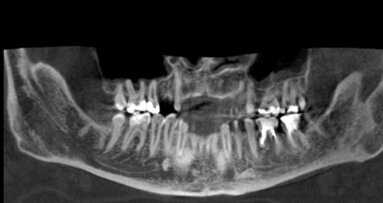
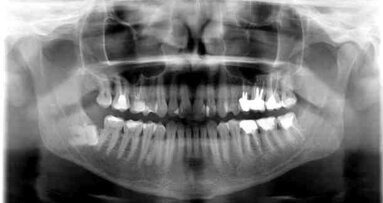
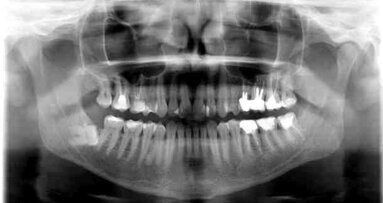
Dwudzielny kanał żuchwy jest anatomiczną odmianą budowy kanału żuchwy oznaczającą, że kanał żuchwy jest podzielony na dwie gałęzie. W ...
Dwudzielny kanał żuchwy jest anatomiczną odmianą budowy kanału żuchwy oznaczającą, że kanał żuchwy jest podzielony na dwie gałęzie. W ...
Autorzy przedstawiają 2 rzadkie przypadki powikłań jatrogennych powstałych podczas wykonywania standardowych zabiegów chirurgii jamy ustnej oraz ...
Autorzy przedstawiają 2 rzadkie przypadki powikłań jatrogennych powstałych podczas wykonywania standardowych zabiegów chirurgii jamy ustnej oraz ...
Webinarium na żywo
czw. 30 kwietnia 2026
1:00 (CET) Warsaw
Dr. Renato Leonardo D.M.D.
Webinarium na żywo
czw. 30 kwietnia 2026
7:00 (CET) Warsaw
Webinarium na żywo
nie. 3 maja 2026
6:00 (CET) Warsaw
Dr. Rickard Brånemark MSc, MD, PhD, Dr. Robert Gottlander DDS
Webinarium na żywo
pon. 4 maja 2026
2:00 (CET) Warsaw
Webinarium na żywo
wto. 5 maja 2026
4:00 (CET) Warsaw
Webinarium na żywo
wto. 5 maja 2026
6:00 (CET) Warsaw
Webinarium na żywo
wto. 5 maja 2026
7:00 (CET) Warsaw
Dr. Maximilian Dobbertin M.Sc



 Austria / Österreich
Austria / Österreich
 Bośnia i Hercegowina / Босна и Херцеговина
Bośnia i Hercegowina / Босна и Херцеговина
 Bułgaria / България
Bułgaria / България
 Chorwacja / Hrvatska
Chorwacja / Hrvatska
 Czechy i Słowacja / Česká republika & Slovensko
Czechy i Słowacja / Česká republika & Slovensko
 Francja / France
Francja / France
 Niemcy / Deutschland
Niemcy / Deutschland
 Grecja / ΕΛΛΑΔΑ
Grecja / ΕΛΛΑΔΑ
 Węgry / Hungary
Węgry / Hungary
 Włochy / Italia
Włochy / Italia
 Holandia / Nederland
Holandia / Nederland
 nordycki / Nordic
nordycki / Nordic
 Polska / Polska
Polska / Polska
 Portugalia / Portugal
Portugalia / Portugal
 Rumunia i Mołdawia / România & Moldova
Rumunia i Mołdawia / România & Moldova
 Słowenia / Slovenija
Słowenia / Slovenija
 Serbia i Czarnogóra / Србија и Црна Гора
Serbia i Czarnogóra / Србија и Црна Гора
 Hiszpania / España
Hiszpania / España
 Szwajcaria / Schweiz
Szwajcaria / Schweiz
 indyk / Türkiye
indyk / Türkiye
 Wielka Brytania i Irlandia / UK & Ireland
Wielka Brytania i Irlandia / UK & Ireland
 Międzynarodowy / International
Międzynarodowy / International
 Brazylia / Brasil
Brazylia / Brasil
 Kanada / Canada
Kanada / Canada
 Ameryka Łacińska / Latinoamérica
Ameryka Łacińska / Latinoamérica
 USA / USA
USA / USA
 Chiny / 中国
Chiny / 中国
 Indie / भारत गणराज्य
Indie / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Wietnam / Việt Nam
Wietnam / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Izrael / מְדִינַת יִשְׂרָאֵל
Izrael / מְדִינַת יִשְׂרָאֵל
 Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
Algieria, Maroko i Tunezja / الجزائر والمغرب وتونس
 Bliski Wschód / Middle East
Bliski Wschód / Middle East









































To post a reply please login or register